- Список сокращений
- Термины и определения
- 1. Краткая информация
- 2. Диагностика
- 3. Лечение
- 4. Реабилитация
- 5. Профилактика
- 6. Дополнительная информация, влияющая на течение и исход заболевания
- Список литературы
- Приложение А1. Состав рабочей группы
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение Б. Алгоритмы ведения пациента
- Приложение В. Информация для пациентов
Уротелиальный рак верхних мочевыводящих путей
Уротелиальный рак верхних мочевыводящих путей
Список сокращений
CIS - carcinoma in situ
FISH – флуоресцентная in situ гибридизация
КТ – компьютерная томография
ЕАУ – Европейская Ассоциация Урологов
СР – степень рекомендаций
УД – уровень доказательности
МДКТУ – мультидетекторная компьютерная урография
МРТ – магнитно-резонансная томорафия
РНУ – радикальная нефроуретерэктомия
УРВМП – уротелиальный рак верхних мочевыводящих путей
ВОЗ – всемирная организация здравоохранения
Термины и определения
Трехстаканная проба мочи – это анализ трёх порций мочи, полученных при однократном мочеиспускании, который позволяет установить локализацию патологического процесса, вызвавшего повышение количества лейкоцитов и/или эритроцитов в моче.
Уретеропиелоскопия – это эндоскопическое вмешательство, которое применяется для визуальной оценки состояния просвета мочеточника и лоханки почки, уточнения наличия в них патологических образований, а также одновременного проведения эндоскопических вмешательств.
Трансуретральная резекция мочевого пузыря – это эндоскопическая операция, которая выполняется с целью удаления новообразования/инородного тела мочевого пузыря с последующим микроскопическим исследованием полученной ткани.
Фотодинамическое исследование – цистоскопия (введение в мочевой пузырь тонкой металлической трубочки с видеокамерой и освещением), которая выполняется с использованием фиолетового света после внутрипузырного введения специального препарата, который проникает в опухолевые клетки и светится ярким цветом.
Нефроуретерэктомия – операция по удалению почки и мочеточника целиком (включая интрамуральный отдел мочеточника), в ряде случаев требующая одновременного выполнения резекции мочевого пузыря.
Неоадъювантная химиотерапия – это вид химиотерапии, проводимый непосредственно перед хирургическим удалением первичной опухоли для улучшения результатов операции или лучевой терапии и для предотвращения образования метастазов.
Адъювантная химиотерапия – это вид химиотерапии, проводимый после полного удаления первичной опухоли, проводимая для устранения возможных метастазов опухоли.
БЦЖ-терапия – иммунотерапия неактивными бактериями туберкулеза проводят в послеоперационном периоде с целью снизить возможность развития рецидива рака мочевого пузыря.
1. Краткая информация
1.1 Определение
Уротелиальный рак занимает 4 место по распространенности злокачественных опухолей после рака простаты (или молочных желез), легкого и колоректального рака [1]. Данный вид опухоли может возникать как в нижних мочевыводящих путях (мочевой пузырь или уретра), так и в верхних (чашечно-лоханочная система почки или мочеточник).
1.2 Этиология и патогенез
Развитие УРВМП отличается от такового при раке мочевого пузыря: 60% УРВМП являются инвазивными на момент установления диагноза, по сравнению с 15-20% при раке мочевого пузыря [4]. Пик заболеваемости УРВМП приходится на седьмую-девятую декаду жизни, УРВМП в три раза чаще встречается у мужчин, чем у женщин [5]. Наследственные случаи УРВМП сочетаются с наследственным неполипозным колоректальным раком.
Курение табака и профессиональная деятельность остаются прямыми факторами риска для развития уротелиального рака. Курение увеличивает риск развития УРВМП с 2,5 до 7 [6]. Профессиональная деятельность, связанная с определенными ароматическими аминами, также является фактором риска (лакокрасочная, текстильная, химическая, нефтяная и угольная промышленность) [7]. У людей, занятых на таких производствах, реализуется карциногенный эффект определенных химических веществ (бензидин и β- нафталин). экспозиция составляет приблизительно 7 лет, с латентным периодом до 20 лет. Риск развития УРВМП после контакта с ароматическими аминами повышается в 8 раз [7].
1.3 Эпидемиология
Рак мочевого пузыря составляет 90-95% среди всех случаев уротелиального рака. Уротелиальный рак верхних мочевыводящих путей (УРВМП) встречается довольно редко и составляет 5-10% от всех случаев уротелиального рака [1,2]. Опухоли лоханки почки встречаются в два раза чаще, чем опухоли мочеточника. В 8- 13% случаев выявляется сочетанный рак мочевого пузыря [3]. Рецидив заболевания в мочевом пузыре встречается у 31-50% пациентов, страдающих УРВМП, в то время, как рецидив в лоханке с контрлатеральной стороны встречается только в 2-6%.
1.4. Классификация МКБ-О
8120/2 Переходно-клеточный рак in situ
8120/3 Переходно-клеточный рак, БДУ
8122/3 Переходно-клеточный рак, веретеноклеточный (саркомоподобный)
8130/1 Папиллярное переходно-клеточное новообразование с низким потенциалом злокачественности
8130/2 Папиллярный переходно-клеточный рак, неинвазивный
8130/3 Папиллярный переходно-клеточный рак
8131/3 Переходно-клеточный рак, микропапиллярный
1.5 Кодирование по МКБ-10
С65 - Злокачественное новообразование почечных лоханок
С66 - Злокачественное новообразование мочеточника
1.6 Классификация
Гистологические типы
Более чем 95% уротелиального рака развивается из уротелия и относится к УРВМП или к раку мочевого пузыря. Что касается УРВМП, морфологические варианты описаны как более часто встречаемые при уротелиальных опухолях почки. Эти варианты относятся к опухолям высокого злокачественного потенциала (high-grade), и соответствуют одному из следующих вариантов: микропапиллярному, светло-клеточному, нейроэндокринному и лимфоэпителиальному. Рак собирательных протоков имеет сходные характеристики с УРВМП благодаря общему эмбриональному происхождению.
Опухоли верхних мочевыводящих путей с неуретральной морфологической структурой довольно редки. Эпидермоидный рак верхних мочевыводящих путей – менее чем в 10% случаев опухолей чашечнолоханочной системы и еще реже при опухолях мочеточника. Другие морфологические типы представлены аденокарциномой (<1%), нейроэндокринным раком и саркомой.
Классификация
Классификация и морфология УРВМП сходна с таковыми при раке мочевого пузыря [4]. Выделяют неинвазивные папиллярные опухоли (папиллярная уротелиальная опухоль с низким злокачественным потенциалом, low-grade папиллярный уротелиальный рак, highgrade папиллярный уротелиальный рак), плоские поражения (carcinoma in situ [CIS]),и инвазивный рак. Все варианты уротелиальных опухолей, описанных для мочевого пузыря, также могут встречаться в верхних мочевыводящих путях.
TNM классификация Union Internationale Contre le Cancer 2009, используемая в данных клинических рекомендациях. Согласно TNM классификации, в качестве регионарных лимфоузлов рассматриваются лимфоузлы ворот почки, парааортальные, паракавальные и, для мочеточника, тазовые лимфоузлы. Сторона поражения не влияет на N классификацию.
TNM классификация 2009 для УРВМП
Т – первичная опухоль
Тх – опервичная опухоль не может быть оценена
Т0 – нет данных за наличие первичной опухоли
Та – неинвазивный папиллярный рак
Tis - carcinoma in situ
Т1 – опухоль вовлекает субэпителиальную соединительную ткань
Т2 – опухоль поражает мышечный слой
Т3 – (почечная лоханка) опухоль прорастает за пределы мышечной оболочки в перипельвикальную жировую ткань или почечную паренхиму (мочеточник) опухоль прорастает за пределы мышечного слоя в периуретеральную жировую клетчатку
Т4 – опухоль вовлекает соседние органы или прорастает через почку в паранефральную клетчатку
N – регионарные лимфоузлы
Nх – регионарные лимфоузлы не могут быть оценены
N0 – нет метастазов в регионарных лимфоузлах
N1 – метастаз в одном лимфоузле 2 см или менее в наибольшем измерении
N2 – метастаз в одном лимфоузле более 2 см, но менее 5 см в наибольшем измерении, или несколько метастазов в лимфатических узлах не более 5 см в наибольшем измерении
N3 – метастазы в лимфоузлах более 5 см в наибольшем измерении.
М – отдаленные метастазы
М0 – нет отдаленных метастазов
М1 – есть отдаленные метастазы
Группировка по стадиям
КР526
| Стадия | T | N | M |
|---|---|---|---|
| 0is, 0a | is,a | 0 | 0 |
| I | 1 | 0 | 0 |
| II | 2 | 0 | 0 |
| III | 3 | 0 | 0 |
| IV | 4 | 0 | 0 |
| 1-4 | 1-3 | 0 | |
| 1 |
2. Диагностика
2.1 Жалобы и анамнез
Рекомендуется сбор жалоб и анамнеза у пациента с целью выявления факторов, которые могут повлиять на выбор тактики лечения.
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIb).
Комментарии: Наиболее распространенным симптомом при УРВМП является макро-/микрогематурия (70-80%). Боль в боку встречается в 20-40% случаев, пальпируемое образование в поясничной области находят в 10-20% случаев. Однако, системные симптомы (измененное состояние здоровья, включая анорексию, потеря веса, недомогание, тошнота, лихорадка, ночная потливость или кашель) должны служить причиной для более детального обследования c целью поиска регионарных метастазов и оценки необходимости проведения периоперационной химиотерапии.
2.2 Физикальное обследование
Рекомендуется физикальный осмотр.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - IV).
2.3 Лабораторная диагностика
Рекомендуется выполнять: развернутые клинический и биохимический анализы крови, включая показатели функции печени (билирубин, АЛТ, АСТ, ЩФ), исследование свёртывающей системы крови, анализ мочи, цитологическое исследование мочи.
Уровень убедительности рекомендаций – С (уровень достоверности доказательств - IV).
Комментарий: Положительный результат цитологического исследования мочи позволяет заподозрить УРВМП при условии, что цистоскопия не выявила изменений и исключена CIS мочевого пузыря и простатической уретры [4]. При диагностике УРВМП цитологическое исследование обладает меньшей чувствительностью, чем при раке мочевого пузыря, даже при high-grade опухолях, и, в идеале, должно выполняться in situ (т.е. из полости почки). Положительный результат цитологического исследования может оказать помощь в стадировании, поскольку ассоциирован с мышечной инвазией и распространении опухолевого процесса за пределы органа.
Выявление молекулярных нарушений при флуоресцентной in situ гибридизации (FISH) становится все более и более популярным для скрининга уротелиального рака, однако результаты пока предварительные. Чувствительность FISH для определения УРВМП сопоставима с таковой при раке мочевого пузыря [11].
Рекомендуется выполнять гистологическое (при невозможности – цитологическое) исследование биопсийного и/или операционного гистологического материала.
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – IIа).
2.4 Инструментальная диагностика
Рекомендуется выполнять МДКТУ при подозрении на УРВМП.
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – IIа).
Комментарии: Мультидетекторная компьютерная урография (МДКТУ) считается золотым стандартом для обследования верхних мочевыводящих путей, заняв место экскреторной урографии (данное исследование должно выполняться при оптимальных условиях, особенно с включением экскреторной фазы, необходимо выполнять сканирование в спиральном режиме (с шагом в 1 миллиметр) до и после ведения контрастного вещества).
Уровень выявления УРВМП считается достаточным для исследований такого типа: 96% чувствительности и 99% специфичности для полиповидных опухолей размером от 5 до 10 мм [8]. Чувствительность снижается до 89% для полиповидных опухолей <5 мм, и составляет 40% для опухолей < 3 мм. При помощи МДКТУ также можно оценить толщину стенки лоханки почки или мочеточника при подозрении на УРВМП. Основной сложностью остается идентификация плоских поражений, которые остаются неопределяемыми до тех пор, пока не разовьется массивная инфильтрация.
Было показано, что выявление гидронефроза на этапе дооперационного обследования ассоциировано с распространенным патологическим процессом и худшими онкологическими результатами [9].
Рекомендуется выполнение МРТ ВМП при невозможности выполнить МДКТУ.
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – II).
Комментарии: Магнитно-резонансная томография (МРТ) показана тем пациентам, которым не удается выполнить МДКТУ. Частота выявления УРВМП при МРТ составляет 75% после введения контрастного вещества для опухолей <2 см. Однако, МРТ с контрастным усилением противопоказана некоторым пациентам со сниженной почечной функцией (клиренс креатинина<30 мл\мин) изза риска развития нефрогенного системного фиброза. МРТ без контрастного усиления считается менее ценной по сравнению с МДКТУ для диагностики УРВМП [10].
Рекомендуется выполнение уретеропиелоскопии при дооперационном обследовании (при технической возможности).
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – II).
Комментарии: Уретероскопия является лучшим методом для диагностики УРВМП. С помощью гибкого уретероскопа можно макроскопически осмотреть мочеточник и большие чашечки почки в 95 % случаев, можно оценить вид опухоли, взять биопсию, определить степень злокачественности опухоли в 90 % случаев с низким уровнем ложноотрицательных результатов. Также с помощью данного метода можно получит материал для цитологического исследования непосредственно из мочеточника, выполнить ретроградную пиелограмму [12].
Уретероскопия особенно полезна когда диагноз неясен, когда предполагается косервативное лечение, или у пациента с единственной почкой. Возможность выполнения уретероскопии следует рассматривать для каждого пациента с УРВМП при дооперационном обследовании. Данные о степени злокачественности опухоли (при биопсии во время уретероскопии), ипсилатеральный гидронефроз и результат цитологического исследования мочи могут помочь принять решение о радикальной нефроуретерэктомии (РНУ) или эндоскопическом лечении.
2.5 Прогностические факторы
Уротелиальный рак верхних мочевыводящих путей с вовлечением мышечного слоя стенки характеризуется плохим прогнозом. 5-летняя специфическая выживаемость составляет <50% при рТ2/рТ3 и <10% при рТ4. В данном разделе коротко описаны современные факторы прогноза [4].
В соответствии с большинством классификаций, первичными прогностическими факторами являются стадия опухолевого процесса и степень злокачественности опухолевых клеток.
Влияние пола на смертность от УРВМП недавно оспорено и более не рассматривается в качестве независимого фактора прогноза. Напротив, возраст пациента до сих пор считается независимым прогностическим фактором поскольку более старший возраст на момент выполнения РНУ ассоциирован с уменьшением опухолево-специфической выживаемости (УД: 3). Однако, пожилой возраст сам по себе не может быть ограничением к агрессивному лечению УРВМП. Большинству пожилых пациентов может быть выполнена РНУ. Это подтверждает тот факт, что возраст сам по себе является неадекватным критерием при оценке отдаленных результатов у пожилых пациентов с УРВМП.
В соответствии с последними данными, первичное расположение опухоли в пределах верхних мочевыводящих путей (т.е. мочеточник или лоханка почки) более не рассматривается как прогностический фактор, в противоположность ране опубликованным сообщениям (УД:3). Это означает, что расположение опухоли (мочеточник или чашечнолоханочная система почки) больше не влияет на установление стадии опухолевого процесса.
Лимфоваскулярная инвазия встречается приблизительно в 20% случаев УРВМП и является независимым предиктором выживаемости. Наличие или отсутствие лимфоваскулярной инвазии должно быть включено в гистологическое заключение после РНУ (УД: 3). Однако, только у пациентов с отсутствием метастазов в лимфоузлы лимфоваскулярная инвазия обладает прогностической ценностью.
Распространенный некроз опухоли является независимым предиктором клинических результатов для пациентов, которые подверглись РНУ. Распространенный некроз опухоли определяется при >10% некроза в опухоли (УД: 3).
Строение опухоли (папиллярная или на широком основании) УРВМП ассоциировано с прогнозом после РНУ. Опухоли на широком основании ассоциированы с худшим прогнозом (УД: 3). Наличие сопутствующей CIS у пациентов с УРВМП, не распространяющимся за пределы органа, ассоциировано с высоким риском рецидива заболевания и опухолевоспецифической смертностью (УД: 3). Также, как и при уротелиальном раке нижних мочевыводящих путей, наличие CIS является независимым предиктором худшего прогноза.
На сегодняшний день ни один из изучаемых молекулярных маркеров не обладает достаточными клиническими и статистическими критериями для внедрения в клиническую практику.
3. Лечение
3.1 Органосохраняющее лечение
Рекомендуется рассматривать возможность органосохраняющего лечебного подхода ТОЛЬКО в учреждениях, обладающих необходимым опытом и техническим оснащением.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
Комментарии: Органосохраняющий подход при low-grade УРВМП позволяет сохранить мочевыводящие пути. Для органосохраняющего лечения существуют абсолютные (почечная недостаточность, единственная функционирующая почка) или элективные (т.е. когда контрлатеральная почка функционирует) показания при low-grade, low-stage опухолях. Выбор метода зависит от технических ограничений, анатомического расположения опухоли и от опыта хирурга.
Уретероскопия
Эндоскопическое лечение может быть осуществлено у тщательно отобранных пациентов в следующих ситуациях [15]:
- требуются гибкий (а не ригидный) уретероскоп, лазерный генератор, щипцы для биопсии (УД: 3).
- пациент должен быть информирован о тщательном, более строгом наблюдении.
- рекомендовано полное удаление опухоли.
Перкутанные манипуляции
Перкутанные лечебные манипуляции могут быть методом выбора при low-grade или неинвазивных опухолях полостей почки.Подобные лечебные опции могут быть применимы для пациентов с low-grade опухолями нижних чашечек, к которым невозможно или очень сложно добраться при уретеропиелоскопии. При подобных процедурах существует риск перфорации и диссеминации опухоли. Однако, данный подход все больше и больше уступает место уретеропиелоскопии в связи с бурным развитием технических возможностей уретеропиелоскопов в последние годы [15].
Адъювантное местное лечение
Инстилляция BCG или митомицина С через перкутанную нефростому в мочевыводящие пути (после полной эрадикации) или даже через мочеточниковый стент является технически выполнимой манипуляцией после консервативного лечения УРВМП или для терапии CIS. Средне- срочные результаты схожи с таковыми при лечении рака мочевого пузыря, однако не подтверждены в долгосрочных исследованиях [16].
3.2 Хирургическое лечение
Рекомендуется применять радикальную нефрутерерэктомию как стандарт хирургического лечения.
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – III).
Комментарии: радикальная нефруретерэктомия (РНУ) с резекцией мочевого пузыря является золотым стандартом лечения УРВМП, независимо от расположения опухоли в верхних мочевыводящих путях (Т1-3N0-1М0) (УД: 3) [13]. РНУ следует выполнять в соответствии с онкологическими принципами, избегая выхода опухолевых масс за пределы мочевыводящих путей в ходе операции.
Следует выполнять иссечение дистального отдела мочеточника и его устья, поскольку существует риск развития рецидива в этой зоне. Недавние публикации о выживаемости после нефроуретерэктомии подтверждают, что удаление дистальной части мочеточника с резекцией мочевого пузыря в области устья имеет преимущество.
В 1952 году McDonald et al. представили технику этой операции. В 1995г был разработан эндоскопический подход для выделения дистальной части мочеточника, также были предложены различные методики для упрощения удаления дистальной части мочеточника: экстирпация, трансуретральная резекция интрамурального отдела, инвагинационные техники. Кроме экстирпации мочеточника, ни одна из предложенных техник не показала преимущества перед резекцией стенки мочевого пузыря в области устья. Отсрочка более 45 дней от момента установления диагноза до удаления опухоли увеличивает риск прогрессирования заболевания.
Рекомендуется выполнить удаление лимфоузлов при выполнении РНУ.
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – III).
Комментарии: Удаление лимфатических узлов при выполнении РНУ обеспечивает лечебный эффект и оптимальное стадирование заболевания. Лимфаденэктомия при рN+ имеет циторедуктивный эффект перед адъювантным лечением (УД: 3). Однако анатомические границы лимфодиссекции еще до конца не определены. Количество удаляемых лимфоузлов зависит от расположения опухоли. Пока еще ни одно исследование не продемонстрировало прямого влияния количества удаленных лимфоузлов на выживаемости. Можно избежать выполнения лимфаденэктомии при Та-Т1 УРВМП.
Рекомендуется избегать вскрытия просвета мочевыводящих путей при РНУ, особенно при выполнении лапароскопической РНУ.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
Комментарии: Последние данные свидетельствуют о эквивалентных результатах между лапароскопическим и открытым доступами. Лапароскопический доступ имеет преимущество перед открытым вмешательством только в отношении функциональных результатов [14].
Необходимо соблюдать несколько правил, чтобы избежать диссеминации опухол и при лапароскопической операции:
- следует избегать нарушения целостности мочевыводящих путей,
- следует избегать прямого контакта инструментов с опухолью,
- для извлечения удаленного препарата следует пользоваться специальными контейнерами,
- почка и мочеточник должны удаляться единым блоком с резецированной стенкой мочевого пузыря в области устья,
- инвазивные, большие (Т3–4 и/или N+/М+), или мультифокальные опухоли являются противопоказанием к лапароскопической РНУ.
3.3 Лечение при наличии отдаленных метастазов
Рекомендуется рассматривать возможность выполнения РНУ в качестве паллиативной помощи при наличии отдаленных метастазов.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
Комментарии: Нет преимуществ РНУ при метастатическом (М+) поражении, хотя данный вариант может быть рассмотрен в качестве паллиативной помощи.
Уровень убедительности рекомендаций - В (уровень достоверности доказательств – III).
Комментарии: Поскольку УРВМП является уротелиальной опухолью, как и при раке мочевого пузыря, используется химиотерапия на основе комбинаций с включением препаратов платины. Основными схемами являются: гемцитабин+цисплатин или гемцитабин+карбоплатин (при клиренсе креатинина <50 мл/мин.):
а) гемцитабин 1000 мг/м2 в/в кап. 1 и 8 дни, цисплатин 80-100 мг/м2 1 день
b) гемцитабин 1000 мг/м2 в/в кап. 1 и 8 дни, карбоплатин AUC3=5 в/в кап. 1 день
Рекомендуется помнить, что значение как неоадъювантной, так и адъювантной ПХТ при УРВМП до конца не определено.
Уровень убедительности рекомендаций - А (уровень достоверности доказательств – Ib).
Комментарии: Только одно исследование подтвердило эффективность неоадъювантной химиотерапии [17]. Ожидаются данные о выживаемости при длительных сроках наблюдения. Предварительные данные подтверждают необходимость такого подхода при лечении УРВМП.
Значение адьювантной терапии после радикального хирургического вмешательства при УРВМП до конца не определено. По отдельным данным адъювантная химиотерапия позволяет добиться снижения относительного риска развития местного рецидива до 50%, но незначительно влияет на общую выживаемость. Не все пациенты смогут получить данный вид лечения из-за сопутствующих заболеваний и нарушения почечной функции после радикального хирургического лечения. На сегодняшний день недостаточно данных для того, чтобы рекомендовать проведение адьювантной химиотерапии после радикальной РНУ, за исключением больных с метастазами в забрюшинных л/узлах, выявленных при плановом гистологическом исследовании после РНУ [17].
3.4 Лучевая терапия
В настоящее время отсутствуют данные с необходимым уровнем доказательности, которые позволяли бы рекомендовать применение лучевой терапии в качестве неоадъювантного или адъювантного метода лечения. Однако, дистанционная лучевая терапия может использоваться с паллиативными целями.
4. Реабилитация
Специфических методов реабилитации не разработано. Следует придерживаться рекомендаций по профилактике хронической почечной недостаточности (ХПН).
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
5. Профилактика
Рекомендуется строгое наблюдение за пациентами с УРВМП после хирургического лечения, поскольку позволяет выявить метахронные опухоли мочевого пузыря (во всех случаях), местный рецидив и отдаленные метастазы (в случае инвазиных опухолей).
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
Комментарии: Если выполнялась РНУ, развитие местного рецидива маловероятно, риск возникновения отдаленных метастазов напрямую зависит от факторов риска, которые были упомянуты ранее.
Рекомендуется оценивать состояние мочевого пузыря при каждом контрольном обследовании.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
Комментарии: Уровень развития рецидива заболевания в мочевом пузыре после лечения первичного УРВМП значительно варьирует от 15 до 50 %. Поэтому, обследование мочевого пузыря должно осуществляться во всех случаях. Наличие рака мочевого пузыря в анамнезе и мультифокальное поражение УРВМП являются факторами риска развития опухоли мочевого пузыря после УРВМП.
Режим наблюдения должен включать цистоскопию и цитологическое исследование мочи по крайней мере в течение 5 лет. Развитие рецидива заболевания в мочевом пузыре не следует рассматривать как появление отдаленных метастазов.
Рекомендуется тщательное наблюдение после выполнения органосохраняющего лечения.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств – IV).
Комментарии: В случае выполнения органосохраняющего лечения, требуется тщательный мониторинг состояния ипсилатеральных мочевыводящих путей ввиду высокого риска развития рецидива. Несмотря на постоянное совершенствование эндоурологической техники, наблюдение за пациентами, пролеченными консервативно, остается сложной задачей, и часто требует выполнения миниинвазивных манипуляций.
6. Дополнительная информация, влияющая на течение и исход заболевания
Критерии оценки качества медицинской помощи
| № | Критерии качества | Оценка выполнения |
|---|---|---|
| 1. | Выполнено ультразвуковое исследование органов малого таза и/или компьютерная томография органов малого таза и/или магнитно-резонансная томография органов малого таза (при установлении диагноза) | Да/Нет |
| 2. | Выполнено ультразвуковое исследование органов брюшной полости (комплексное) и забрюшинного пространства, компьютерная томография органов брюшной полости и забрюшинного пространства и/или магнитно-резонансная томография органов брюшной полости и забрюшинного пространства (при установлении диагноза) | Да/Нет |
| 3. | Выполнена рентгенография органов грудной клетки и/или компьютерная томография органов грудной клетки (при установлении диагноза) | Да/Нет |
| 4. | Проведена профилактика инфекционных осложнений антибактериальными лекарственными препаратами при хирургическом вмешательстве (при отсутствии медицинских противопоказаний) | Да/Нет |
| 5. | Выполнено морфологическое и/или иммуногистохимическое исследование препаратов удаленных тканей (при хирургическом вмешательстве) | Да/Нет |
| 6. | Выполнена химиотерапия и/или иммунотерапия и/или таргетная терапия и/или лучевая терапия при наличии морфологической верификации диагноза (при химиотерапии и/или иммунотерапии и/или таргетной терапии и/или лучевой терапии) | Да/Нет |
| 7. | Выполнена дозиметрическая верификация рассеивающего плана (при лучевой терапии) | Да/Нет |
| 8. | Выполнено общий (клинический) анализ крови развернутый не более чем за 5 дней до начала курса химиотерапии и/или иммунотерапии и/или таргетной терапии и/или лучевой терапии | Да/Нет |
| 9. | Начата таргетная терапия и/или иммунотерапия и/или первый курс химиотерапии не позднее 60 дней от момента выявления метастатической болезни (при наличии медицинских показаний и отсутствии медицинских противопоказаний) | Да/Нет |
Список литературы
- Siegel, R.L., et al. Cancer statistics, 2015. CA Cancer J Clin, 2015. 65: 5.
- Munoz, J.J., et al. Upper tract urothelial neoplasms: incidence and survival during the last 2 decades. J Urol, 2000. 164: 1523.
- Cosentino, M., et al. Upper urinary tract urothelial cell carcinoma: location as a predictive factor for concomitant bladder carcinoma. World J Urol, 2013. 31: 141.
- Babjuk, M., et al. EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder, the 2011 update. Eur Urol, 2011. 59: 997.
- Shariat, S.F., et al. Gender differences in radical nephroureterectomy for upper tract urothelial carcinoma. World J Urol, 2011. 29: 481.
- Crivelli, J.J., et al. Effect of smoking on outcomes of urothelial carcinoma: a systematic review of the literature. Eur Urol, 2014. 65: 742.
- Colin, P., et al. Environmental factors involved in carcinogenesis of urothelial cell carcinomas of the upper urinary tract. BJU Int, 2009. 104: 1436.
- Ito, Y., et al. Preoperative hydronephrosis grade independently predicts worse pathological outcomes in patients undergoing nephroureterectomy for upper tract urothelial carcinoma. J Urol, 2011. 185: 1621
- Hurel, S., et al. Influence of preoperative factors on the oncologic outcome for upper urinary tract urothelial carcinoma after radical nephroureterectomy. World J Urol, 2015. 33: 335.
- Takahashi, N., et al. Gadolinium enhanced magnetic resonance urography for upper urinary tract malignancy. J Urol, 2010. 183: 1330.
- Reynolds, J.P., et al. Comparison of urine cytology and fluorescence in situ hybridization in upper urothelial tract samples. Cancer Cytopathol, 2014. 122: 459.
- Rojas, C.P., et al. Low biopsy volume in ureteroscopy does not affect tumor biopsy grading in upper tract urothelial carcinoma. Urologic oncology, 2013. 31: 1696.
- Margulis, V., et al. Outcomes of radical nephroureterectomy: a series from the Upper Tract Urothelial Carcinoma Collaboration. Cancer, 2009. 115: 1224.
- Walton, T.J., et al. Oncological outcomes after laparoscopic and open radical nephroureterectomy: results from an international cohort. BJU Int, 2011. 108: 406.
- Cutress, M.L., et al. Ureteroscopic and percutaneous management of upper tract urothelial carcinoma (UTUC): systematic review. BJU Int, 2012. 110: 614.
- Giannarini, G., et al. Antegrade perfusion with bacillus Calmette-Guerin in patients with non-muscle-invasive urothelial carcinoma of the upper urinary tract: who may benefit? Eur Urol, 2011. 60: 955.
- Leow, J.J., et al. A Systematic Review and Meta-analysis of Adjuvant and Neoadjuvant Chemotherapy for Upper Tract Urothelial Carcinoma. Eur Urol, 2014. 66: 529.
Приложение А1. Состав рабочей группы
- Волкова М.И., д.м.н., ведущий научный сотрудник урологического отделения ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» Минздрава России;
- Матвеев В.Б., профессор, д.м.н., заведующий урологическим отделением ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» Минздрава России;
- Носов Д.А., д.м.н., заведующий отделением противоопухолевой лекарственной терапии Центральной клинической больницы Управления Делами Президента РФ;
- Хмелевский Е.В., профессор, д.м.н., заведующий отделом лучевой терапии ФГБУ «Московский научно-исследовательский онкологический институт им. П.А.Герцена» Минздрава России.
Конфликта интересов нет
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
- Врачи-онкологи
- Врачи-урологи
- Врачи-радиотерапевты
- Врачи-химиотерапевты
- Студенты медицинских ВУЗов, ординаторы и аспиранты
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме уротелиального рака верхних мочевыводящих путей в РФ и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Таблица П1 – Уровни достоверности доказательств в соответствии с классификацией Агентства по политике медицинского обслуживания и исследований (AHCPR, 1992)
| Уровни доказательств | Описание |
|---|---|
| Ia | Доказательность, основанная на мета-анализе рандомизированных контролируемых исследований |
| Ib | Доказательность, основанная как минимум на одном рандомизированном контролируемом исследовании с хорошим дизайном |
| IIa | Доказательность, основанная как минимум на одном крупном нерандомизированном контролируемом исследовании |
| IIb | Доказательность, основанная как минимум на одном квазиэкспериментальном исследовании с хорошим дизайном |
| III | Доказательность, основанная на неэкспериментальных описательных исследованиях с хорошим дизайном, типа сравнительных исследований, корреляционных исследований и исследований случаев-контроль |
| IV | Доказательность, основанная на мнении экспертов, на опыте или мнении авторов |
Таблица П2 – Уровни убедительности рекомендаций в соответствии с классификацией Агентства исследований и оценки качества медицинского обслуживания (AHRQ, 1994)
| Уровни убедительности рекомендаций | Уровни доказательств | Описание |
|---|---|---|
| A | Ia, Ib | Доказательность, основанная как минимум на одном рандомизированном контролируемом исследовании с хорошим дизайном |
| B | IIa, IIb, III | Доказательность, основанная на хорошо выполненных нерандомизированных клинических исследованиях |
| C | IV | Доказательность, основанная на мнении экспертов, на опыте или мнении авторов. Указывает на отсутствие исследований высокого качества |
Методы, использованные для формулирования рекомендаций – консенсус экспертов.
Экономический анализ
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
- Внешняя экспертная оценка
- Внутренняя экспертная оценка
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами, которые попросили прокомментировать, прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей-детских онкологов первичного звена в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался и вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультации и экспертная оценка: Проект рекомендаций рецензирован также независимыми экспертами, которых попросили прокомментировать, прежде всего, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Обновления клинических рекомендаций: актуализация проводится не реже чем один раз в три года с учетом появившейся новой информации о диагностике и тактике ведения пациентов с данной патологией. Решение об обновлении принимает МЗ РФ на основе предложений, представленных медицинскими профессиональными некоммерческими организациями. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология изучается для того, чтобы убедиться в ее достоверности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что в свою очередь влияет на силу, вытекающих из нее рекомендаций.
Приложение Б. Алгоритмы ведения пациента
Схема 1. Блок-схема лечения пациента с уротелиальным раком верхних мочевыводящих путей
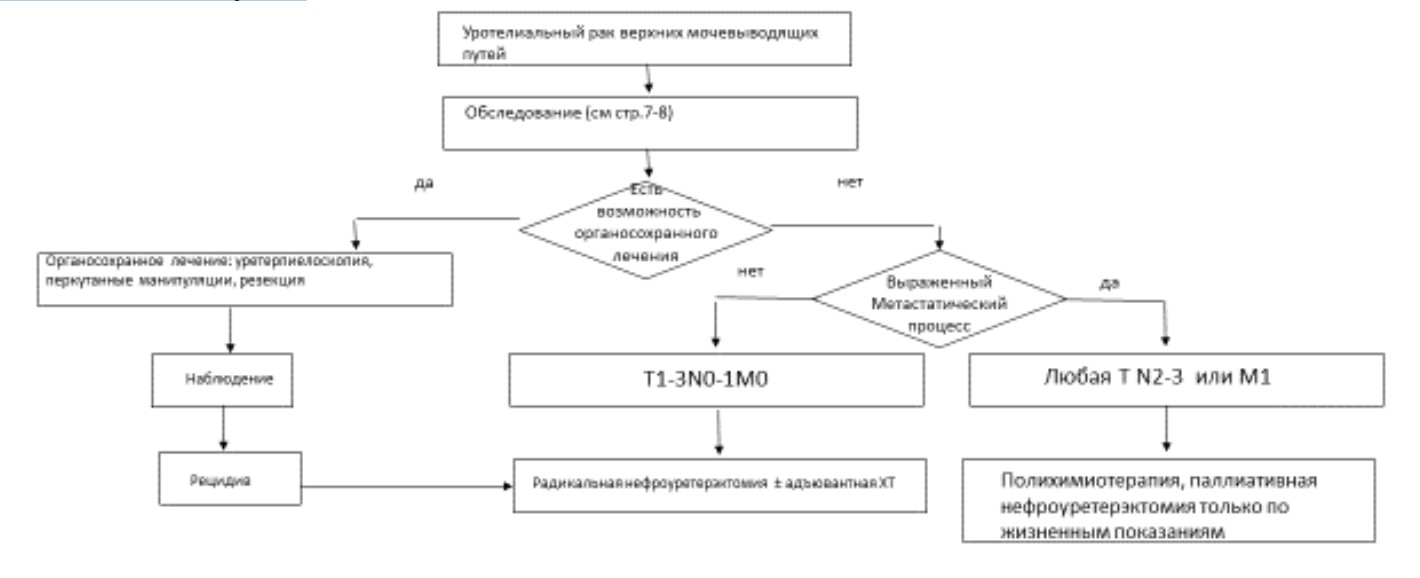
Приложение В. Информация для пациентов
Рекомендации при осложнениях химиотерапии - связаться с химиотерапевтом.
1. При повышении температуры тела 38°C и выше
Начать прием антибиотиков: по рекомендации химиотерапевта.
2. При стоматите
- Диета – механическое, термическое щажение;
- Частое полоскание рта (каждый час) – ромашка, кора дуба, шалфей, смазывать рот облепиховым (персиковым) маслом;
- Обрабатывать полость рта по рекомендации химиотерапевта.
3. При диарее
- Диета – исключить жирное, острое, копченое, сладкое, молочное, клетчатку. Можно нежирное мясо, мучное, кисломолочное, рисовый отвар. Обильное питье.
- Принимать препараты по рекомендации химиотерапевта.
4. При тошноте
Принимать препараты по рекомендации химиотерапевта.