Первый опыт применения суперимпульсного волоконного тулиевого лазера для контактного разрушения камней общего желчного и главного панкреатического протока
Первый опыт применения суперимпульсного волоконного тулиевого лазера для контактного разрушения камней общего желчного и главного панкреатического протока
Цель представления клинического наблюдения: продемонстрировать возможность использования нового суперимпульсного фиброволоконного тулиевого лазера при контактной внутрипротоковой литотрипсии у пациентов с холедохолитиазом и вирсунголитиазом.
Основные положения: Представлены два клинических наблюдения успешного разрушения крупных конкрементов желчных и панкреатических протоков с использованием суперимпульсного фиброволоконного тулиевого лазера FiberLase U2 фирмы НТО «ИРЭ-Полюс» (Россия) во время пероральной транспапиллярной холангиопанкреатикоскопии у пациентов, у которых проведение традиционного малоинвазивного лечения холедохо- и вирсунголитиаза было технически невозможно. Пациент 72 лет поступил экстренно с клинической картиной острой механической желтухи и холангита, в анамнезе эндоскопическая папиллосфинктеротомия (ЭПСТ) и билио-дуоденальное стентирование пластиковым стентом в связи с технической невозможностью проведения литотрипсии и литоэкстракции. Попытка экстракорпоральной литотрипсии была неэффективна, и на 3-и сутки после ее проведения выполнено повторное ретроградное вмешательство и эндоскопическая контактная лазерная литотрипсия под контролем пероральной транспапиллярной холангиоскопии с FiberLase U2. Пациент 50 лет поступил с клинической картиной хронического калькулезного панкреатита. В анамнезе ЭПСТ, вирсунготомия, панкреатическое стентирование пластиковым стентом. Первым этапом эндоскопического лечения стало удаление инкрустированного панкреатического стента, ретроградная панкреатикография, вирсунготомия, бужирование зоны сужения терминального отдела вирсунгова протока механическими дилататорами и дополнительная баллонная дилатация области вирсунготомии и панкреатической стриктуры с помощью дилатационного баллона. Попытки внутрипротоковой механической литотрипсии не были успешны. Проведена контактная лазерная литотрипсия с использованием нового суперимпульсного фиброволоконного тулиевого лазера. Использование представляемого методического подхода обеспечило полную санацию протоковой системы без повреждения слизистой оболочки.
Заключение: первый в нашей стране и мире опыт использования суперимпульсного фиброволоконного тулиевого лазера для контактной литотрипсии крупных конкрементов общего желчного и главного панкреатического протока завершился полным клиническим успехом.
Ключевые слова: ЭРХПГ, холангиоскопия, панкреатикоскопия, холедохолитиаз, вирсунголитиаз, внутрипротоковая контактная литотрипсия, суперимпульсный фиброволоконный тулиевый лазер
Конфликт интересов: авторы заявляют об отсутствии конфликтов интересов.
Для цитирования: Будзинский С.А., Шаповальянц С.Г., Федоров Е.Д., Воробьева Е.А., Свирин М.Ю., Маляров М.Г., Чернякевич П.Л., Платонова Е.Н. Первый опыт применения суперимпульсного волоконного тулиевого лазера для контактного разрушения камней общего желчного и главного панкреатического протока. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2021;31(2):54–64. https://doi.org/10.22416/1382-4376-2021-31-2-54-64
В последние годы малоинвазивные эндоскопические методики стали «золотым стандартом» при лечении холедохо- и вирсунголитиаза, в том числе при выявлении крупных конкрементов желчевыводящих путей и протоков поджелудочной железы. При этом с различным успехом используются такие методы, как баллонная дилатация области предварительно проведенной эндоскопической папиллосфинктеротомии (ЭПСТ) и/или вирсунготомии (ВТ) с последующей литоэкстракцией; внутрипротоковая механическая литотрипсия, дистанционная ударноволновая литотрипсия (ДУВЛ) с последующим эндоскопическим удалением фрагментов камней [1, 2]. В то же время в последние 15 лет все большее количество авторов рекомендуют в случаях выявления крупных конкрементов желчных и панкреатических протоков, которые характеризуются невозможностью выполнения вышеперечисленных методов литотрипсии и удаления, применение техники эндоскопической контактной литотрипсии при пероральной транспапиллярной холангиопанкреатикоскопии [1, 3]. При этом примерно одинаковой эффективностью обладают как лазерная, так и электрогидравлическая литотрипсии — 99 и 96,7 % соответственно [4].
Долгое время основным вариантом контактной внутрипротоковой лазерной литотрипсии было использование гольмиевого лазера, который широко применяли как в эндоскопии панкреатобилиарной зоны, так и в урологии при уролитиазе [5] и в челюстно-лицевой хирургии в лечении сиалолитиаза [6]. В 2013–2014 годах стали появляться первые публикации о возможностях нового вида лазера, разработанного российскими учеными, в основе действия которого находятся ионы редкоземельного металла тулия (№ 69), который так же, как и его сосед в Периодический системе химических элементов — гольмий (№ 67) относится к лантаноидам. Тулиевые лазеры имеют более высокую степень поглощения их излучения водой по сравнению с гольмиевыми (1,94 нм у тулиевого лазера против 2,1 нм у гольмиевого).
Появление волоконной архитектуры тулиевого лазера дало еще более высокую степень поглощения хромофором-водой (мишенью, поглощающей лазерное излучение) лазерной энергии, что обеспечило бóльшую способность передачи энергии окружающей водосодержащей среде. В то же время появление суперимпульсного режима, то есть возможности модулировать выходящие импульсы в более широком диапазоне по сравнению с классическими импульсными лазерами по количеству энергии в единичном импульсе (от 0,025 до 6 Дж), по его продолжительности (от 0,2 до 60 мс) и частоте (от 1 до 1600 Гц), обеспечило более дозированное и прецизионное воздействие на водосодержащую среду, в частности на конкременты, находящиеся в ней. Ширина диапазона настроек указанных показателей влияет на способность лазера адаптироваться под конкретную клиническую ситуацию. Превосходство именно в этих параметрах и определяет высокую эффективность волоконных суперимпульсных лазеров: до 4 раз более высокое КПД, а также до 20 раз более широкий диапазон настройки основных параметров.
В первых сообщениях по применению тулиевого лазера максимальный акцент был сделан на выполнении абляции преимущественно в области урологии [7]. Несколько позднее данный вид лазера стали применять и для литотрипсии уролитов различной плотности, причем наибольшее количество сообщений об успешном использовании данной методики составляют отечественные публикации [7–9]. В 2018 г. на медицинском рынке появился аппарат FiberLase U2 фирмы НТО «ИРЭ-Полюс» российского производства, в основе которого лежит воздействие принципиально нового суперимпульсного фиброволоконного тулиевого лазера на различные ткани и конкременты. В исследовании E.X. Keller et al., посвященном использованию этого устройства при фрагментации крупных уролитов, продемонстрирована возможность успешного дробления конкремента высокой плотности размерами 30ђ20ђ20 мм, располагающегося в почечной лоханке, режимами «Распыление» и «Попкорнинг» за общее время 37 минут [10]. Из данного наблюдения авторы делают вывод, что эти режимы помогают фрагментировать камни любого диаметра до столь мелких частиц, что подобный подход позволяет отказаться от использования экстракторов и корзинок.
До настоящего времени в доступной нам отечественной литературе мы не встретили публикаций о возможности выполнения эндоскопической контактной лазерной литотрипсии с использованием суперимпульсного волоконного тулиевого лазера в лечении холедохо- и вирсунголитиаза. В публикациях зарубежных авторов мы нашли единственное клиническое наблюдение: случай применения тулиевого лазера в лечении холедохолитиаза [11] с применением аппарата Quanta System Srl. (Италия).
Представляем первый успешный опыт проведения подобных вмешательств у двух пациентов с крупными конкрементами общего желчного протока (ОЖП) и главного панкреатического протока (ГПП).
Клинический случай № 1
Пациент П. 72 лет поступил в нашу клинику в ноябре 2020 г. в экстренном порядке с клинической картиной острой неполной механической желтухи и холангита. В октябре 2019 г. в одном из стационаров г. Москвы по поводу острой механической желтухи, обусловленной крупным камнем ОЖП, пациенту была выполнена ЭПСТ и билио-дуоденальное стентирование пластиковым стентом в связи с технической невозможностью проведения литотрипсии и литоэкстракции. Желтуха разрешилась; до настоящего поступления пациент за врачебной помощью не обращался.
В нашей клинике больной был дообследован. По данным лабораторных методов выявлен лейкоцитоз до 11,9ђ109/л, а также повышение уровня общего билирубина до 63,5 мкмоль/л, фракция прямого билирубина составила 42,4 мкмоль/л. Данные ультразвукового исследования (УЗИ) органов брюшной полости подтвердили наличие конкремента размером 28ђ16 мм и стента в расширенном до 18 мм ОЖП. В неувеличенном желчном пузыре также определялись множественные камни различного диаметра.
Для достижения адекватного дренирования билиарного тракта пациенту в нашей клинике предполагалось выполнение внутрипротоковой механической литотрипсии. При проведении дуоденоскопии отмечена полная обструкция пластикового стента замазкообразными массами, при этом область ЭПСТ располагалась в нижнем крае крупного дивертикула. В ходе вмешательства после удаления стента из просвета холедоха отмечено поступление гноевидного содержимого и нитей фибрина.
По данным эндоскопической ретроградной холангиографии (ЭРХГ) (рис. 1) в дистальных отделах ОЖП визуализирован крупный конкремент овальной формы размерами 36ђ18 мм, практически полностью перекрывающий просвет холедоха, а также расширение общего печеночного и общего желчного протоков выше обструкции до 18–19 мм и умеренная дилатация внутрипеченочных протоков. При этом в терминальном отделе на протяжении 1 см отмечено относительное сужение просвета ОЖП до 5 мм, что, наиболее вероятно, было связано с длительно существующим ХЛ и наличием крупного дивертикула. Желчный пузырь и пузырный проток достоверно не контрастировались.
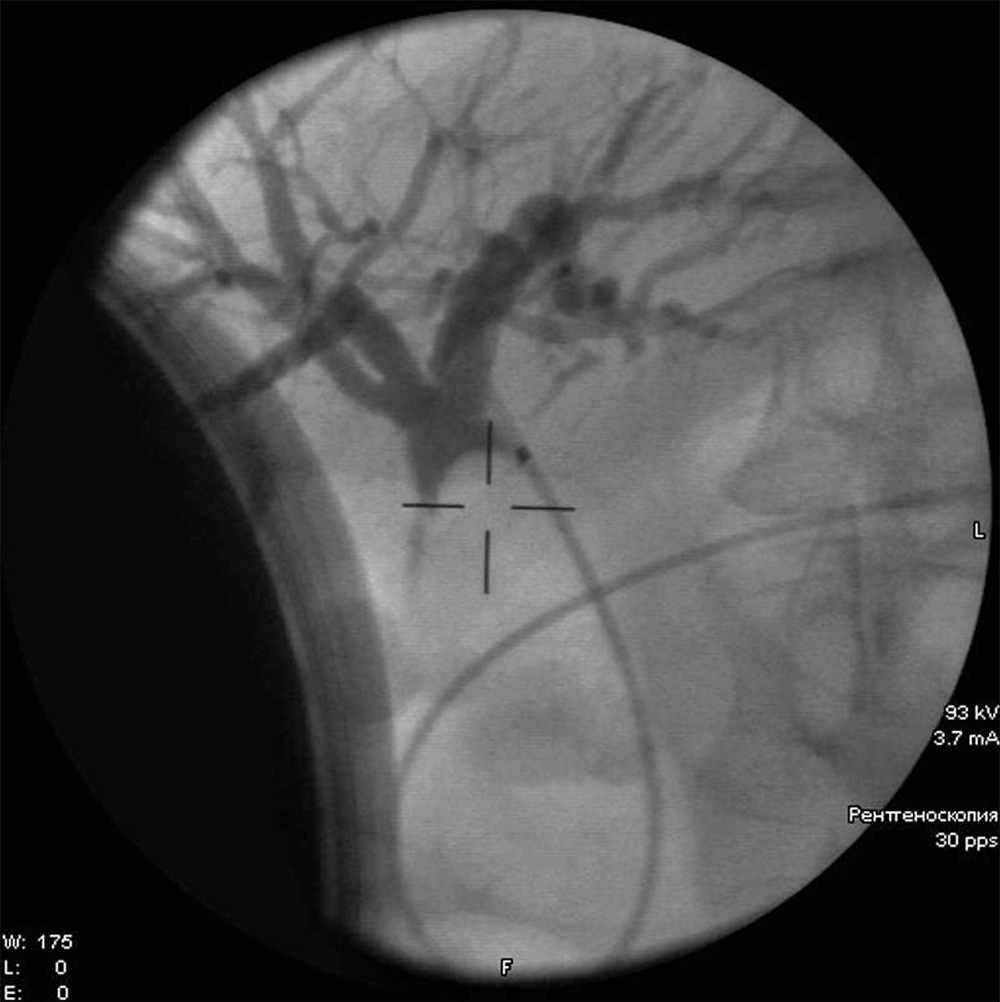
Рис. 1. Холангиограмма пациента с крупным конкрементом в просвете расширенного общего желчного протока
Принято решение о проведении дополнительной баллонной дилатации области ранее выполненной ЭПСТ и терминальных отделов ОЖП, механической внутрипротоковой литотрипсии и литоэкстракции, а также назобилиарного дренирования.
С помощью баллона диаметром 13–14–15 мм и длиной 5 см фирмы Boston Scientific (США) была успешно осуществлена баллонная дилатация области ЭПСТ (рис. 2a–c). Однако попытка механической литотрипсии оказалась безуспешной ввиду невозможности завести литотриптор выше конкремента и захватить его. Учитывая интраоперационную ситуацию, а также наличие клинико-эндоскопических проявлений острого холангита, было принято решение о выполнении назобилиарного дренирования и проведении дистанционной ударноволновой литотрипсии (ДУВЛ) после разрешения клинической картины холангита (рис. 2d).
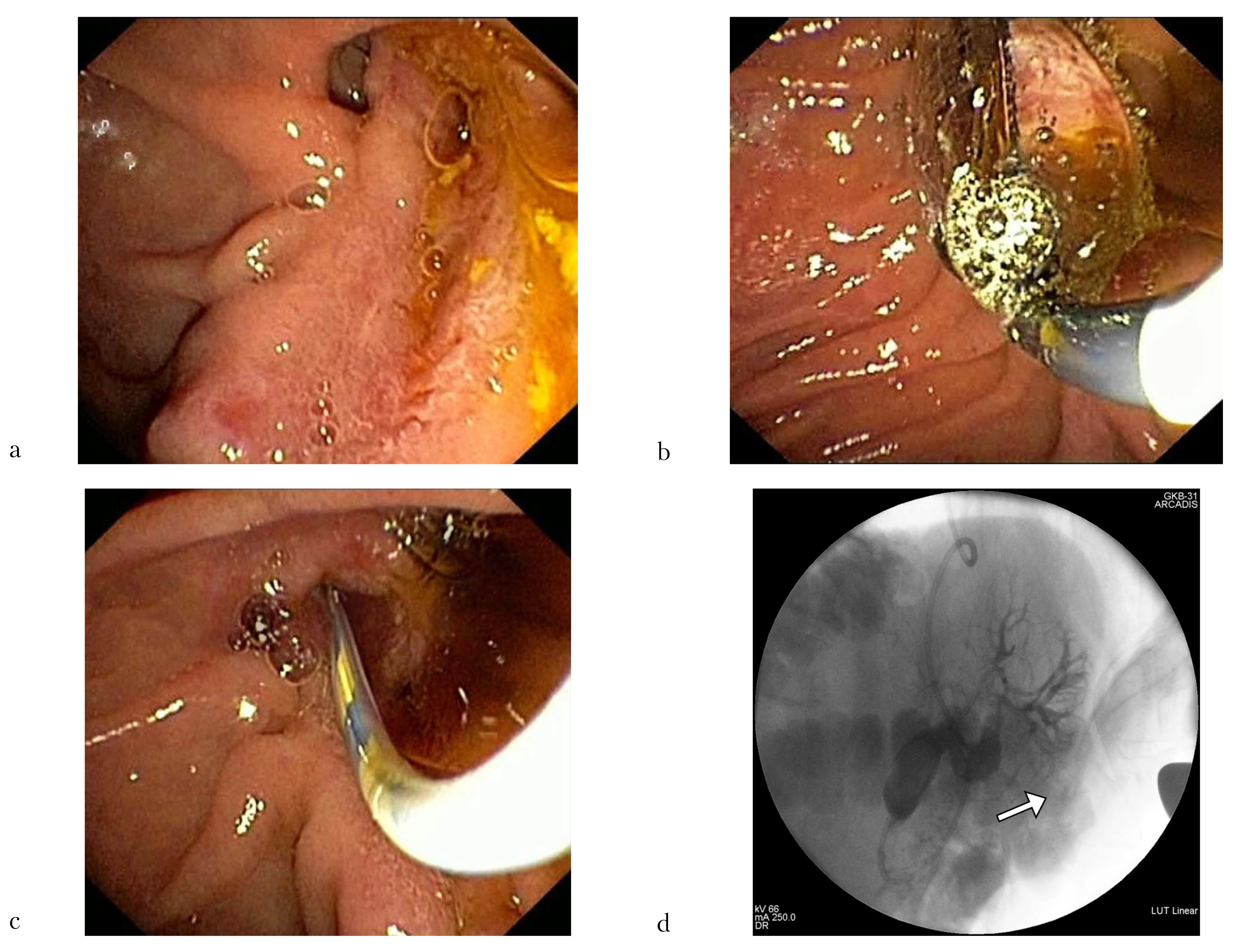
Рис. 2: a — устье холедоха до баллонной дилатации (эндофото); b — баллонная дилатация (эндофото); c — устье холедоха после баллонной дилатации (эндофото); d — назобилиарный дренаж, установленный в просвет ОЖП, где в дистальных отделах определяется крупный конкремент — указан стрелкой (холангиограмма)
На 5-е сутки после первичного вмешательства и после констатации полного разрешения клинической картины холангита с применением аппарата Dornier Comact Delta II (Германия) был осуществлен один сеанс ДУВЛ, в ходе которого под рентген-навигацией на конкремент было осуществлено воздействие 3100 импульсов преимущественно максимальной интенсивности до 5 уровня (52,0 мПа, 0,72 мДж/кв. мм, 52,0 мДж, совокупная энергия 120,25 Дж). По завершении сеанса было отмечено лишь минимальное разрушение дистального края камня, заключавшееся в появлении некоторой нечеткости его контуров, и смещение конкремента в область общего печеночного протока при введении контрастного препарата (рис. 3).

Рис. 3. Крупный конкремент холедоха во время сеанса дистанционной ударно-волновой литотрипсии (ДУВЛ) (холангиограмма)
Послеоперационный период протекал гладко. Однако, учитывая малую эффективность экстракорпоральной литотрипсии, на 3-и сутки после ее проведения было принято решение о выполнении повторного ретроградного вмешательства с целью выполнения эндоскопической контактной лазерной литотрипсии под контролем пероральной транспапиллярной холангиоскопии с применением нового суперимпульсного фиброволоконного тулиевого лазера FiberLase U2 (Россия).
После удаления назобилиарного дренажа и ретроградной канюляции ОЖП с помощью аппарата Spy-Glass DS II фирмы Boston Scientific (США) была проведена холангиоскопия, при которой была визуализирована неровная, фрагментарно изъеденная часть дистального края конкремента светло-коричневого цвета, занимающего практически весь просвет общего желчного протока. После заполнения просвета билиарного тракта стерильным физиологическим раствором через инструментальный канал холедохоскопа было проведено лазерное волокно диаметром 200 микрон. После этого с использованием тулиевого лазера в режиме «Распыление» была выполнена литотрипсия нижнего полюса камня с постепенным увеличением параметров частоты с 40 до 60 Гц и средней мощности с 8 до 12 Вт при энергии в импульсе 0,2 Дж (рис. 4a). После разрушения поверхностных слоев конкремента визуализировалось его наиболее плотное «ядро» светлого цвета (рис. 4b).
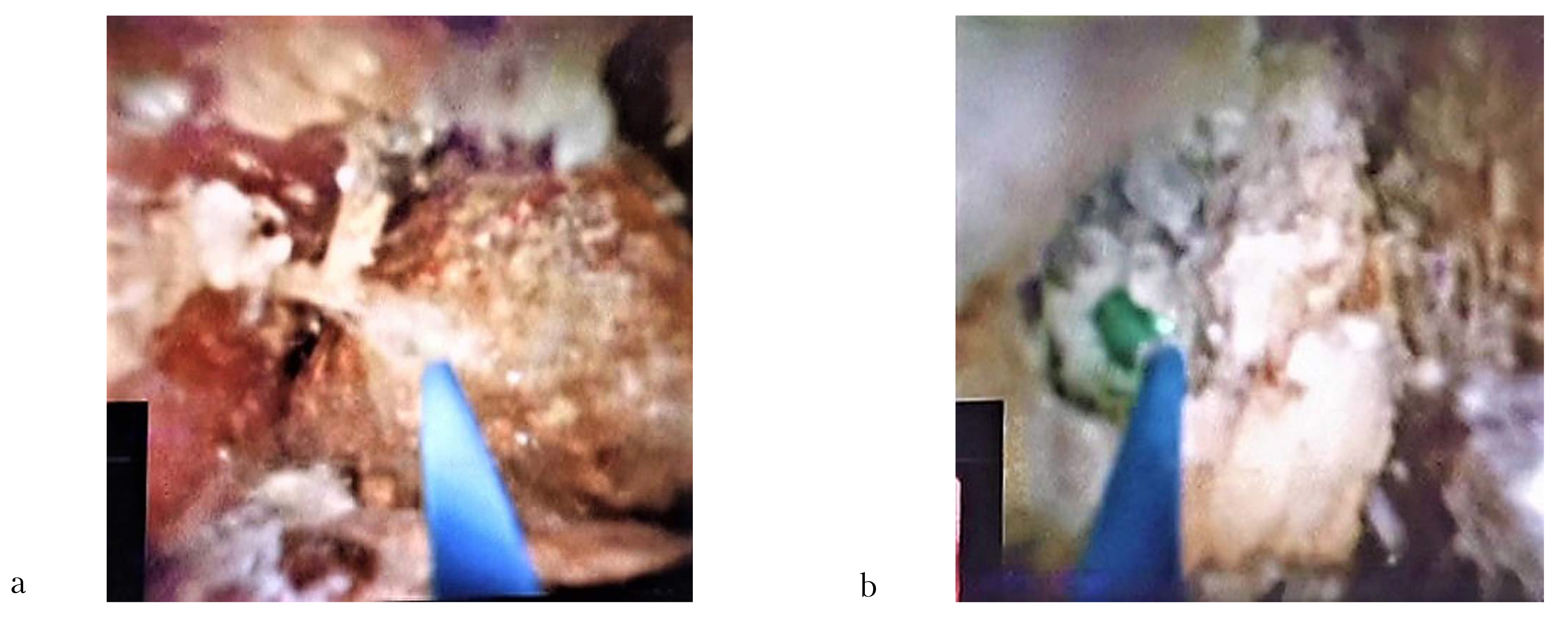
Рис. 4: a — разрушение нижнего полюса конкремента (эндофото); b — визуализирована центральная часть конкремента (эндофото)
Затем с помощью лазерного волокна большего диаметра (400 микрон) в попеременно используемых режимах «Распыление» и «Попкорнинг» была разрушена центральная часть конкремента и выполнена его фрагментация (размеры полученных осколков составили от 4 до 12 мм) (рис. 5). Во время вмешательства были отмечены единичные кратковременные (не более 1 секунды) попадания лазерного луча на стенку ОЖП, при этом какихлибо изменений со стороны слизистой холедоха выявлено не было.
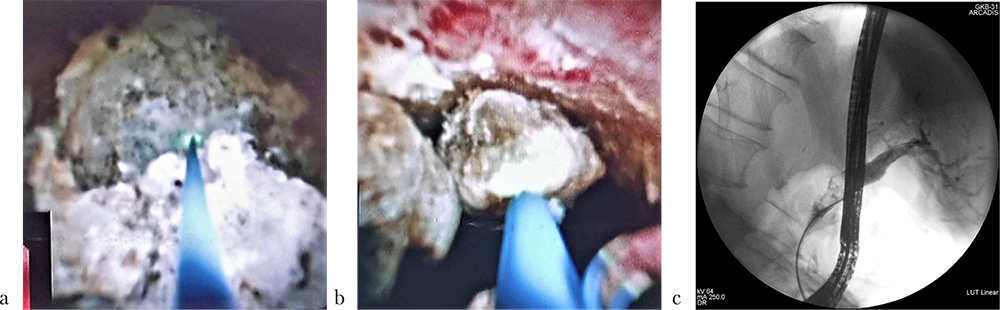
Рис. 5: a — разрушение центральной части конкремента (эндофото); b — один из фрагментов разрушенного конкремента (эндофото); c — разрушенный на фрагменты крупный конкремент (холангиограмма)
После этого с помощью механического литотриптора фирмы Boston Scientific (США) диаметром 3 см наибольший фрагмент камня был успешно захвачен и разрушен, а все остальные части и осколки раздробленного лазером конкремента без технических трудностей удалены с помощью корзинки Дормиа и экстракционного баллона. При контрольной обтурационной холангиографии с использованием раздутого ревизионного баллона была констатирована полная санация билиарного тракта (рис. 6).
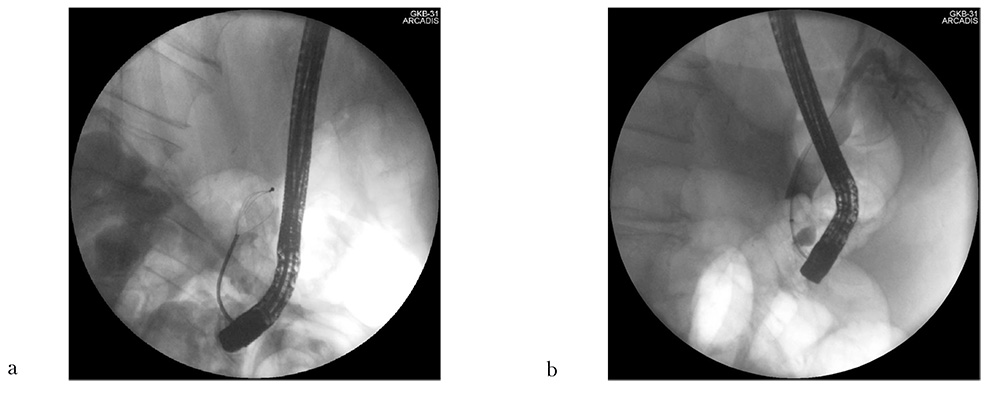
Рис. 6: a — механическая литотрипсия наиболее крупного фрагмента конкремента после лазерной литотрипсии (холангиограмма); b — контрольная ревизия экстракционным баллоном с выполнением обтурационной холангиографии (холангиограмма)
По окончании литоэкстракции пациенту была проведена дополнительная контрольная пероральная транспапиллярная холангиоскопия с осмотром всех отделов желчного дерева от устья ОЖП до сегментарных протоков правой и левой доли печени. При этом была отмечена гиперемия слизистой оболочки холедоха в дистальных его отделах, что, наиболее вероятно, возникло на фоне длительного нахождения в данной области конкремента, а также ранее установленных пластикового стента и назобилиарного дренажа. Иных изменений, а также нарушений целостности стенок протока, связанных с выполнением контактной литотрипсии тулиевым лазером, выявлено не было. При проведении холангиоскопии также была констатирована полная санация желчного дерева.
Продолжительность всей операции составила 55 минут, при этом непосредственно лазерная литотрипсия конкремента заняла 18 минут.
Послеоперационный период протекал гладко в условиях хирургического отделения с отчетливой положительной динамикой, и на 3-и сутки после завершающего вмешательства больной был выписан из стационара. Через 1,5 месяца, в январе 2021 г., в плановом порядке пациенту была выполнена лапароскопическая холецистэктомия.
Клинический случай № 2
Пациент Т. 50 лет поступил в наш стационар с клинической картиной хронического калькулезного панкреатита и верифицированного крупного вирсунголитиаза.
Из анамнеза известно, что хронический панкреатит алиментарного генеза у больного был впервые диагностирован около 20 лет назад, в октябре 2019 г. при проведении УЗИ брюшной полости был выявлен крупный вирсунголит. В ноябре 2019 г., в связи с усилением болевого синдрома и похуданием на 8 кг за 5 месяцев пациенту по месту жительства (Волгоград) была выполнена ЭРХПГ, ЭПСТ, вирсунготомия, баллонная дилатация области вирсунготомии, литоэкстракция нескольких мелких конкрементов ГПП и панкреатическое стентирование пластиковым стентом. При контрольном УЗИ в ноябре 2020 г. отмечено увеличение размеров вирсунголита с 15 до 18 мм, в связи с чем больной был направлен в нашу клинику.
Пациент был дообследован в объеме эндосонографии, при которой было выявлено расширение главного панкреатического протока в головке — до 13 мм, в теле — до 10 мм, в хвосте — до 6 мм, а также наличие в его просвете крупного конкремента размером 18ђ12 мм неправильной продолговатой формы, локализованного в 1–1,5 см выше устья вирсунгова протока (рис. 7). Таким образом, диагноз хронического калькулезного панкреатита, крупного ВЛ и выраженной дилатации ГПП был подтвержден.
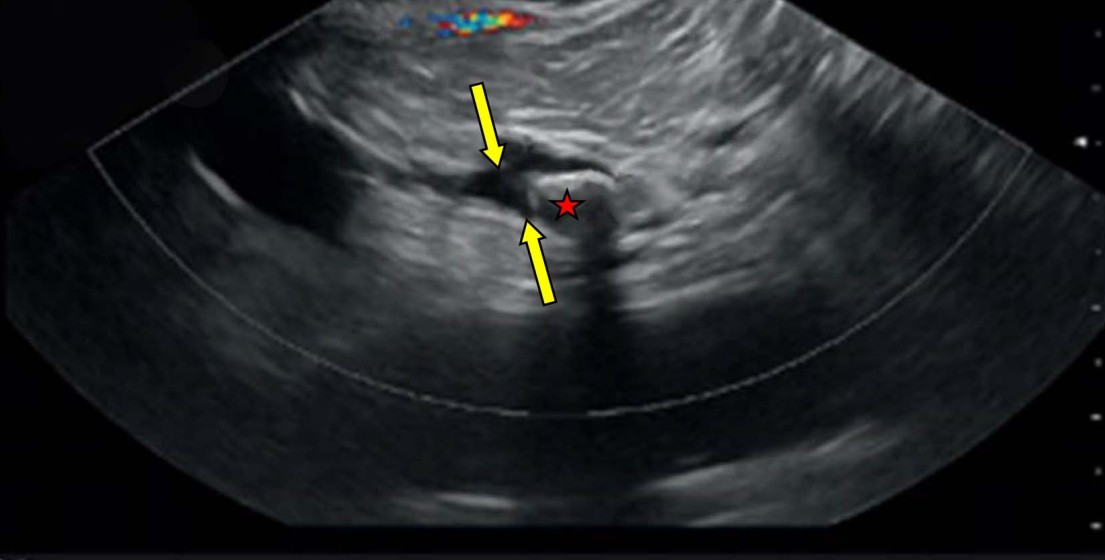
Рис. 7. Эндосонография поджелудочной железы конвексным эхоэндоскопом — в просвете расширенного вирсунгова протока (указан стрелками) крупный конкремент с яркой акустической тенью (отмечен звездочкой)
Первым этапом эндоскопического лечения было проведено удаление инкрустированного панкреатического стента, ретроградная панкреатикография, по результатам которой было выявлено относительное сужение ГПП в терминальном отделе до 2–3 мм на протяжении 3–4 мм, что, вероятнее всего, являлось одним из проявлений хронического панкреатита и пусковым механизмом развития ВЛ. Также на расстоянии около 1 см от устья ГПП визуализирован конкремент неправильной овальной формы с неровными краями размерами 18ђ12 мм (рис. 8a). Нами была выполнена дополнительная ВТ, бужирование зоны сужения терминального отдела вирсунгова протока механическими дилататорами Soehendra от 4 до 9 Фр фирмы Cook (США) и дополнительная баллонная дилатация области вирсунготомии и панкреатической стриктуры с помощью дилатационного баллона диаметром 6–8 мм и длиной 2 см фирмы Boston Scientific (США) (рис. 8b–d). После этого были предприняты многочисленные попытки захвата вирсунголита с целью проведения его внутрипротоковой механической литотрипсии, которые, однако, оказались безуспешны по причине невозможности проведения литотриптора выше камня (рис. 8e). В связи с этим была проведена диагностическая пероральная транспапиллярная панкреатикоскопия с целью визуального осмотра конкремента и оценки технической возможности выполнения лазерной литотрипсии. При визуальном изучении вирсунголита выяснено, что он занимает практически весь просвет ГПП, имеет неровные, шероховатые края и выраженно плотную структуру (рис. 9a). Учитывая размеры, локализацию и наличие адекватного доступа к конкременту, было принято решение о целесообразности проведения контактной лазерной литотрипсии с использованием нового суперимпульсного фиброволоконного тулиевого лазера.
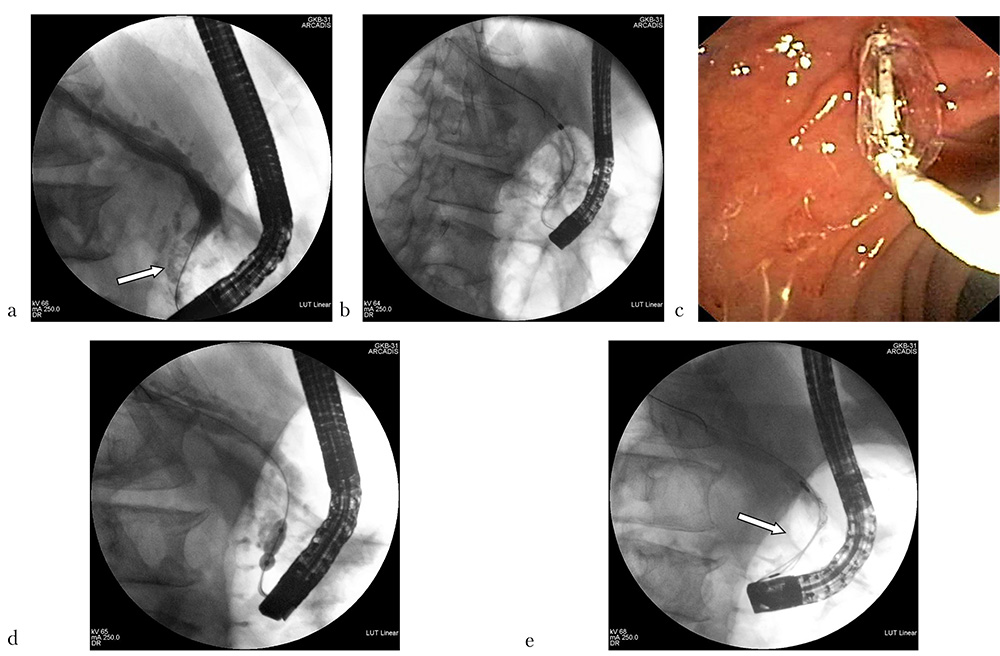
Рис. 8: a — выраженно расширенный ГПП с конкрементом в проекции головки ПЖ — конкремент указан стрелкой (панкреатикограмма); b — бужирование ГПП механическим дилататором (панкреатикограмма); c — баллонная дилатация устья и терминальных отделов ГПП (эндофото); d — баллонная дилатация стриктуры терминальных отделов ГПП (панкреатикограмма); e — попытка механической литотрипсии, при которой отмечена техническая невозможность захвата вирсунголита, конкремент — указан стрелкой (панкреатикограмма)
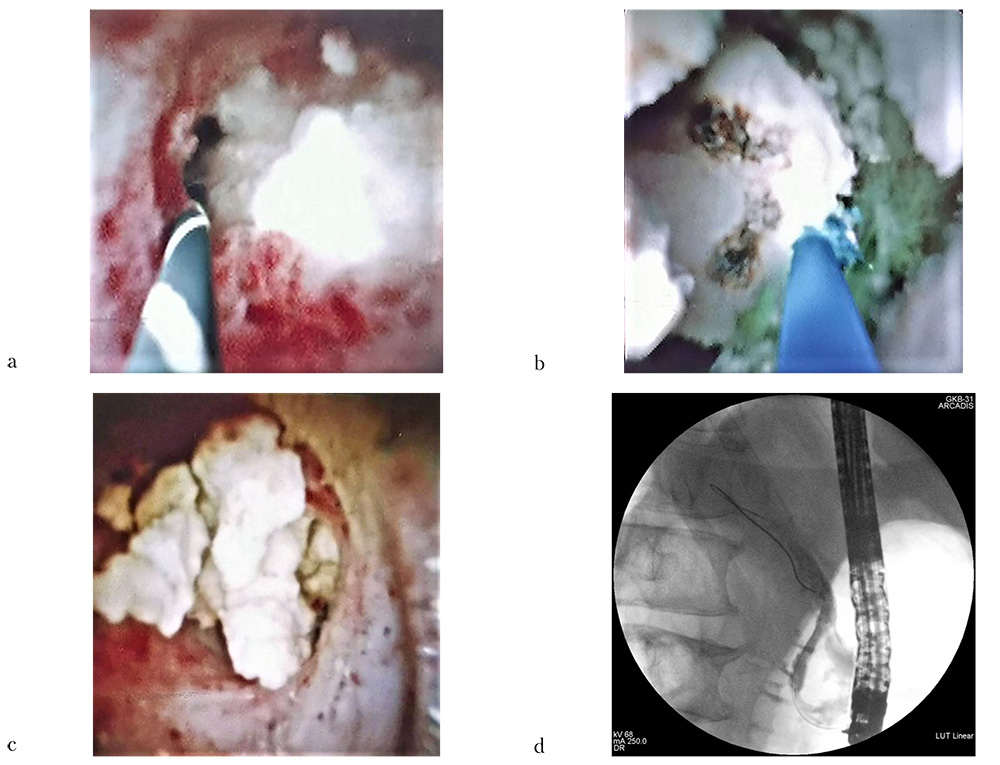
Рис. 9: a — вирсунголит, занимающий практически весь просвет ГПП (эндофото); b — разрушение «поверхностного» слоя вирсунголита (эндофото); c — фрагменты разрушенного «ядра» конкремента (эндофото); d — контрольное контрастирование ГПП (панкреатикограмма)
На 4-е сутки после первичного вмешательства пациент был оперирован повторно. После проведения аппарата Spy-Glass DS II фирмы Boston Scientific (США) в просвет ГПП при помощи тулиевого суперимпульсного фиброволоконного лазера FiberLase U2 с использованием лазерного волокна диаметром 400 микрон при безопасных настройках частоты и средней мощности от 60 до 100 Гц и от 6 до 10 Вт соответственно при энергии в импульсе 0,1 Дж был разрушен поверхностный слой конкремента в режиме «Распыление» (рис. 9b). После этого выполнена фрагментация основного «ядра» вирсунголита в режиме «Попкорнинг» с постепенным увеличением параметров частоты и средней мощности с 40 до 60 Гц и с 8 до 12 Вт соответственно при энергии в импульсе 0,2 Дж (рис. 9c).
При этом камень был полностью фрагментирован, что позволило в дальнейшем санировать просвет вирсунгова протока с помощью корзинки Дормиа, ревизионного баллончика и промывания стерильным физиологическим раствором. При выполнении контрольной ретроградной панкреатикографии и пероральной транспапиллярной панкреатикоскопии ГПП был осмотрен на всем протяжении от хвоста до устья: конкрементов, а также повреждений слизистой оболочки панкреатического протока выявлено не было (рис. 9d).
Продолжительность всего эндоскопического вмешательства составила 115 минут, при этом на саму процедуру лазерной литотрипсии вирсунголита пришлось 70 минут. В послеоперационном периоде пациент находился в хирургическом отделении, где ему проводилась комплексная консервативная терапия в объеме адекватного обезболивания (анальгин, папаверин, глюкозо-новокаиновая смесь), антисекреторной поддержки (октреотид), внутривенного введения гастропротекторов (рабепразол) и инфузионной терапии (NaCl 0,9 %, Glucosae 5 %) в общем объеме 1,5 л. Учитывая отсутствие осложнений и положительную динамику в состоянии больного, на 3-и сутки после оперативного вмешательства он был выписан из стационара.
Заключение
Таким образом, первый в нашей стране и мире опыт использования суперимпульсного фиброволоконного тулиевого лазера для контактной литотрипсии через холангио-панкреатикоскоп крупных конкрементов общего желчного и главного панкреатического протока завершился полным клиническим успехом. Использование данного методического подхода оказалось максимально эффективным, обеспечив полную санацию протоковых систем при использовании подобранных установок работы лазера, оптимальные режимы которых еще предстоит отработать в зависимости от размера и состава билиарных и панкреатических конкрементов. При этом разрушение поверхностных слоев камней начинало происходить уже при первых воздействиях на него лазерного волокна даже на минимальных установках мощности и частоты, но в то же время травмирования стенки протоковых систем не наблюдалось даже при кратковременном попадании на них действующего луча благодаря его небольшой глубине проникновения (около 0,2 мм).
Литература
- Buxbaum J.L., Abbas Fehmi S.M., Sultan S., Fishman D.S., Qumseya B.J., Cortessis V.K., et al. ASGE guideline on the role of endoscopy in the evaluation and management of choledocholithiasis. Gastrointest Endosc. 2019;89(6):1075–105.e15. DOI: 10.1016/j.gie.2018.10.001
- Komanduri S., Thosani N., Abu Dayyeh B.K., Aslanian H.R., Enestvedt B.K., Manfredi M., et al. Cholangiopancreatoscopy. Gastrointest Endosc. 2016;84(2):209– 21. DOI: 10.1016/j.gie.2016.03.013
- McCarty T.R., Sobani Z., Rustagi T. Per-oral pancreatoscopy with intraductal lithotripsy for difficult pancreatic duct stones: a systematic review and meta-analysis. Endosc Int Open. 2020;8(10):E1460–70. DOI: 10.1055/a-1236-3187
- Brewer Gutierrez O.I., Bekkali N.L.H., Raijman I., Sturgess R., Sejpal D.V., Aridi H.D., et al. Efficacy and Safety of Digital Single-Operator Cholangioscopy for Difficult Biliary Stones. Clin Gastroenterol Hepatol. 2018;16(6):918–26.e1. DOI: 10.1016/j.cgh.2017.10.017
- Becker B., Gross A.J., Netsch C. Ho:YaG laser lithotripsy: recent innovations. Curr Opin Urol. 2019;29(2):103–7. DOI: 10.1097/MOU.0000000000000573
- Durbec M., Dinkel E., Vigier S., Disant F., Marchal F., Faure F. Thulium-YAG Laser Sialendoscopy for Parotid and Submandibular Sialolithiasis. Lasers Surg Med. 2012;44(10):783–6. DOI: 10.1002/lsm.22094. Epub 2012 Dec 6.
- Enikeev D.V., Glybochko P.V., Okhunov Z., Alyaev Y.G., Rapoport L.M., Tsarichenko D., et al. Retrospective Analysis of Short-Term Outcomes after Monopolar Versus Laser Endoscopic Enucleation of the Prostate: A Single Center Experience. J Endourol. 2018;32(5):417–23. DOI: 10.1089/end.2017.0898
- Gao B., Bobrowski A., Lee J. A scoping review of the clinical efficacy and safety of the novel thulium fiber laser: The rising star of laser lithotripsy. Can Urol Assoc J. 2021;15(2):56–66. DOI: 10.5489/cuaj.6804
- Kronenberg P., Traxer O. The laser of the future: reality and expectations about the new thulium fiber laser-a systematic review. Transl Androl Urol. 2019;8(Suppl 4):S398- S417. doi: 10.21037/tau.2019.08.01.
- Keller E.X., Coninck V., Vinnichenko V., Chiron P., Doizi S., Guseynov M., et al. Thulium fiber laser for lithotripsy of large renal stones: initial experience. J Urology. 2019;201(4s):e88. DOI: 10.1097/01. JU.0000555081.47403.44
- Mutignani M., Dioscoridi L., Italia A., Forti E., Pugliese F., Cintolo M., et al. Thulium laser to manage a difficult biliary lithiasis: a first case report. 2020;52(3):E112–3. DOI: 10.1055/a-0983-8278